Intercambiador de calor de carcasa y tubos
Los balances de energía resultan fundamentales para establecer las variaciones de energía que se producen durante un proceso industrial, o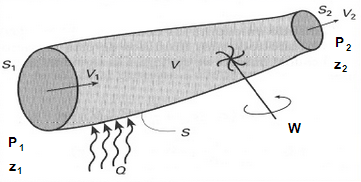 bien para determinar los requerimientos energéticos de una determinada operación o proceso industrial. Algunos ejemplos son los siguientes:
bien para determinar los requerimientos energéticos de una determinada operación o proceso industrial. Algunos ejemplos son los siguientes:
- Energía que es necesario suministrar a un calderín de ebullición en una columna de destilación.
- Calor que se debe suministrar o retirar a través del encamisado de un reactor para realizar una reacción endotérmica o exotérmica.
- Calor que debemos suministrar a una caldera en un ciclo termodinámico de Rankine.
- Potencia requerida para bombear un fluido a una determinada altura.
En cualquiera de estas situaciones es imprescindible plantear y resolver balances de energía de foma análoga a como se han realizado en secciones anteriores los balances de materia.
Todo balance de energía responde a la siguiente ecuación de conservación:
[Acumulación de energía]=[Entrada de energía]-[Salida de energía]+[Generación de energía]-[Consumo de energía]
Esta ecuación resume la conservación de la energía, donde la entrada y salida de energía se refieren a las corrientes de entrada y salida de un sistema, la generación de energía se relaciona con la producción o consumo interno de energía, y el almacenamiento de energía representa cualquier cambio en la energía interna del sistema.
Tipos de Energía:
Energía Interna (U): Energía total contenida en un sistema, incluyendo energía cinética y potencial de las partículas.
Energía Cinética (K): Energía asociada al movimiento de las partículas.
Energía Potencial (φ): Energía asociada a la posición de las partículas en un campo gravitatorio.
Energía de Flujo (H): Energía internal de un fluido sumado al trabajo de flujo (U+PV)
Flujo de Energía:
Calor (Q): Energía transferida entre un sistema y su entorno debido a una diferencia de temperatura.
Trabajo (W): Energía transferida entre un sistema y su entorno debido a una fuerza aplicada a través de una distancia.
Balances de Energía sin Reacción Química:
En sistemas sin reacción química, el balance de energía se simplifica, centrándose en la conservación de la energía total, incluyendo la entrada y salida de calor y trabajo.
Balances de Energía con Reacción Química:
En sistemas con reacción química, se deben considerar los cambios en la energía debido a la entalpía de reacción, cambios en la energía interna y otros términos relacionados con la generación o consumo de energía durante las reacciones.
Eficiencia Térmica:
La eficiencia térmica de un proceso se define como la relación entre el trabajo útil producido y la entrada total de calor.


