Una disolución acuosa de hidróxido de sodio contiene 20$\%$ en masa de NaOH. Se desea producir una disolución al 8$\%$ de NaOH diluyendo un flujo de una disolución al 20$\%$ con un flujo de agua pura.
a) Calcular los cocientes (g de $H_2O$/g de la disolución de alimentación) y (g de la disolución producto/g de la disolución de alimentación).
b) Determinar las velocidades de flujo de la disolución de alimentación y del agua de dilución necesarias para producir 2310 $lb_m/min$ de la disolución al 8$\%$
Solución:
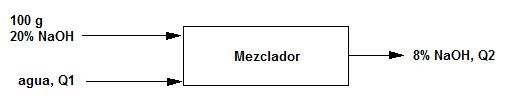
- Base de cálculo 100 g de disolución
- Balance global total: $100 + Q_1=Q_2$
- Balance global parcial $(NaOH): 100\cdot 0.2=Q_2\cdot 0.08$
- Resolviendo el sistema: $Q_2=250\;g$de NaOH y $Q_1=150\;g$ de agua.
a) 150 g de agua/100 g de alimentación = 1.5
- 250 g de disolución al 8$\%$/100 g de alimentación = 2.5
b) Utilizamos un factor de escala: $\frac{2310}{250}=9.24\;lb/gmin$
- lb/min de alimentación: 924
- lb/min de agua: 1386


