Inicialmente se mezcla etano con oxígeno para obtener un gas de 80$\%$ de $C_2H_6$ y 20$\%$ de $O_2$ que después se quema con un 200$\%$ de exceso de aire. El 80$\%$ del etano pasa a $CO_2$, 10$\%$ pasa a CO y 10$\%$ permanece sin quemarse. Calcular la composición del gas de escape (combustión) sobre una base húmeda.
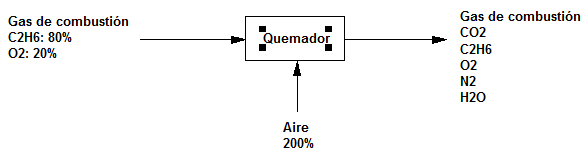
Base de cálculo 100 mol-kg de gas de combustión.
$C_2H_6 + 7/2O_2 \rightarrow 2CO_2 +2H_2O$
$C_2H_6+5/2O_2\rightarrow 2CO + 3H_2O$
- Entrada:
- Cálculo del oxígeno teórico, oxígeno requerido para la combustión completa: 280 mol-kg
- Oxígeno requerido (aire): 280-20=260
- Oxígeno que entra por el aire (200$\%$ en exceso): 780 mol-kg
- Nitrógeno que entra: 2930 mol-kg.
- Oxígeno consumido: 224+20=244 mol-kg.
- Salida:
- Dióxido de carbono:128 mol-kg.
- Monóxido de carbono: 16 mol-kg.
- Agua: 192+24=216 mol-kg.
- Oxígeno: 780+20-244=556 mol-kg
- Nitrógeno: 2930 mol-kg.
- $C_2H_6$: 8 mol-kg


